- الدين القيم
- قال تعالي في دينه القيم :
- لَمْ يَكُنِ الَّذِينَ كَفَرُوا مِنْ أَهْلِ الْكِتَابِ وَالْمُشْرِكِينَ مُنْفَكِّينَ حَتَّى تَأْتِيَهُمُ الْبَيِّنَةُ (1) رَسُولٌ مِنَ اللَّهِ يَتْلُو صُحُفًا مُطَهَّرَةً (2) فِيهَا كُتُبٌ قَيِّمَةٌ (3) وَمَا تَفَرَّقَ الَّذِينَ أُوتُوا الْكِتَابَ إِلَّا مِنْ بَعْدِ مَا جَاءَتْهُمُ الْبَيِّنَةُ (4) وَمَا أُمِرُوا إِلَّا لِيَعْبُدُوا اللَّهَ مُخْلِصِينَ لَهُ الدِّينَ حُنَفَاءَ وَيُقِيمُوا الصَّلَاةَ وَيُؤْتُوا الزَّكَاةَ وَذَلِكَ دِينُ الْقَيِّمَةِ (5) إِنَّ الَّذِينَ كَفَرُوا مِنْ أَهْلِ الْكِتَابِ وَالْمُشْرِكِينَ فِي نَارِ جَهَنَّمَ خَالِدِينَ فِيهَا أُولَئِكَ هُمْ شَرُّ الْبَرِيَّةِ (6) إِنَّ الَّذِينَ آَمَنُوا وَعَمِلُوا الصَّالِحَاتِ أُولَئِكَ هُمْ خَيْرُ الْبَرِيَّةِ (7)/سورة البينة
- قُلْ إِنَّنِي هَدَانِي رَبِّي إِلَى صِرَاطٍ مُسْتَقِيمٍ دِينًا قِيَمًا مِلَّةَ إِبْرَاهِيمَ حَنِيفًا وَمَا كَانَ مِنَ الْمُشْرِكِينَ (161)/سورة الأنعام
- قُلْ إِنَّنِي هَدَانِي رَبِّي إِلَى صِرَاطٍ مُسْتَقِيمٍ دِينًا قِيَمًا مِلَّةَ إِبْرَاهِيمَ حَنِيفًا وَمَا كَانَ مِنَ الْمُشْرِكِينَ (161) قُلْ إِنَّ صَلَاتِي وَنُسُكِي وَمَحْيَايَ وَمَمَاتِي لِلَّهِ رَبِّ الْعَالَمِينَ (162) لَا شَرِيكَ لَهُ وَبِذَلِكَ أُمِرْتُ وَأَنَا أَوَّلُ الْمُسْلِمِينَ (163) قُلْ أَغَيْرَ اللَّهِ أَبْغِي رَبًّا وَهُوَ رَبُّ كُلِّ شَيْءٍ وَلَا تَكْسِبُ كُلُّ نَفْسٍ إِلَّا عَلَيْهَا وَلَا تَزِرُ وَازِرَةٌ وِزْرَ أُخْرَى ثُمَّ إِلَى رَبِّكُمْ مَرْجِعُكُمْ فَيُنَبِّئُكُمْ بِمَا كُنْتُمْ فِيهِ تَخْتَلِفُونَ (164) وَهُوَ الَّذِي جَعَلَكُمْ خَلَائِفَ الْأَرْضِ وَرَفَعَ بَعْضَكُمْ فَوْقَ بَعْضٍ دَرَجَاتٍ لِيَبْلُوَكُمْ فِي مَا آَتَاكُمْ إِنَّ رَبَّكَ سَرِيعُ الْعِقَابِ وَإِنَّهُ لَغَفُورٌ رَحِيمٌ (165)/الانعام
- فَأَقِمْ وَجْهَكَ لِلدِّينِ حَنِيفًا فِطْرَةَ اللَّهِ الَّتِي فَطَرَ النَّاسَ عَلَيْهَا لَا تَبْدِيلَ لِخَلْقِ اللَّهِ ذَلِكَ الدِّينُ الْقَيِّمُ وَلَكِنَّ أَكْثَرَ النَّاسِ لَا يَعْلَمُونَ (30)/سورة الروم
- فَأَقِمْ وَجْهَكَ لِلدِّينِ الْقَيِّمِ مِنْ قَبْلِ أَنْ يَأْتِيَ يَوْمٌ لَا مَرَدَّ لَهُ مِنَ اللَّهِ يَوْمَئِذٍ يَصَّدَّعُونَ (43)/سورة الروم
- إِنَّ عِدَّةَ الشُّهُورِ عِنْدَ اللَّهِ اثْنَا عَشَرَ شَهْرًا فِي كِتَابِ اللَّهِ يَوْمَ خَلَقَ السَّمَاوَاتِ وَالْأَرْضَ مِنْهَا أَرْبَعَةٌ حُرُمٌ ذَلِكَ الدِّينُ الْقَيِّمُ فَلَا تَظْلِمُوا فِيهِنَّ أَنْفُسَكُمْ وَقَاتِلُوا الْمُشْرِكِينَ كَافَّةً كَمَا يُقَاتِلُونَكُمْ كَافَّةً وَاعْلَمُوا أَنَّ اللَّهَ مَعَ الْمُتَّقِينَ (36)/سورة التوبة
- وَاتَّبَعْتُ مِلَّةَ آَبَائِي إِبْرَاهِيمَ وَإِسْحَاقَ وَيَعْقُوبَ مَا كَانَ لَنَا أَنْ نُشْرِكَ بِاللَّهِ مِنْ شَيْءٍ ذَلِكَ مِنْ فَضْلِ اللَّهِ عَلَيْنَا وَعَلَى النَّاسِ وَلَكِنَّ أَكْثَرَ النَّاسِ لَا يَشْكُرُونَ (38) يَا صَاحِبَيِ السِّجْنِ أَأَرْبَابٌ مُتَفَرِّقُونَ خَيْرٌ أَمِ اللَّهُ الْوَاحِدُ الْقَهَّارُ (39) مَا تَعْبُدُونَ مِنْ دُونِهِ إِلَّا أَسْمَاءً سَمَّيْتُمُوهَا أَنْتُمْ وَآَبَاؤُكُمْ مَا أَنْزَلَ اللَّهُ بِهَا مِنْ سُلْطَانٍ إِنِ الْحُكْمُ إِلَّا لِلَّهِ أَمَرَ أَلَّا تَعْبُدُوا إِلَّا إِيَّاهُ ذَلِكَ الدِّينُ الْقَيِّمُ وَلَكِنَّ أَكْثَرَ النَّاسِ لَا يَعْلَمُونَ (40) يَا صَاحِبَيِ السِّجْنِ أَمَّا أَحَدُكُمَا فَيَسْقِي رَبَّهُ خَمْرًا وَأَمَّا الْآَخَرُ فَيُصْلَبُ فَتَأْكُلُ الطَّيْرُ مِنْ رَأْسِهِ قُضِيَ الْأَمْرُ الَّذِي فِيهِ تَسْتَفْتِيَانِ (41)/يوسف
- الْحَمْدُ لِلَّهِ الَّذِي أَنْزَلَ عَلَى عَبْدِهِ الْكِتَابَ وَلَمْ يَجْعَلْ لَهُ عِوَجًا (1) قَيِّمًا لِيُنْذِرَ بَأْسًا شَدِيدًا مِنْ لَدُنْهُ وَيُبَشِّرَ الْمُؤْمِنِينَ الَّذِينَ يَعْمَلُونَ الصَّالِحَاتِ أَنَّ لَهُمْ أَجْرًا حَسَنًا (2) مَاكِثِينَ فِيهِ أَبَدًا (3) وَيُنْذِرَ الَّذِينَ قَالُوا اتَّخَذَ اللَّهُ وَلَدًا (4)/سورة الكهف
الجامعة
نداء الحق
نداء سورة الطلاق/نداء الحق لامة الاسلام-فاعتبروا يا أولي الأبصار
///
حسبنا الله ونعم الوكيل في كل مفتر ظالم
بحث هذه المدونة الإلكترونية
الجمعة، 12 ديسمبر 2025
لَمْ يَكُنِ الَّذِينَ كَفَرُوا مِنْ أَهْلِ الْكِتَابِ وَالْمُشْرِكِينَ مُنْفَكِّينَ حَتَّى تَأْتِيَهُمُ الْبَيِّنَةُ (1) رَسُولٌ مِنَ اللَّهِ يَتْلُو صُحُفًا مُطَهَّرَةً (2) فِيهَا كُتُبٌ قَيِّمَةٌ ..
لا تَقُومُ السَّاعَةُ حتَّى يَنْزِلَ الرُّومُ بالأعماق أو بدابق
لا تَقُومُ السَّاعَةُ حتَّى يَنْزِلَ الرُّومُ بالأعماق أو بدابق *******
إجمالي مرات مشاهدة الصفحة {كانين13}
أرشيف المدونة الإلكترونية{كانين}
-
▼
2023
(45)
-
▼
أغسطس 2023
(11)
- العلماء ومسؤلياتهم الخطيرة علي ضياع دين الله في نف...
- التينبا كرورس Tinea cruris) الكي بالماء المغلي
- بانوراما مناعية//
- السنن الكبرى (سنن النسائي الكبرى) قام علي إيجاد م...
- وفاة النبي صلى الله عليه وسلم لأحمد بن شعيب النسا...
- الاستجابات المناعية المتخصصة: الأجسام المضادَّة ال...
- الكركم نباتات طبية
- السبانخ
- الزنجبيل
- ما هو معني الإشهاد كتكليف حاسم من الله لعبادة?
- القائمة الرئيسية مقدمةالطب هو فرع من علوم الصحة و...
-
▼
سبتمبر 2023
(34)
- أسماء الله الحسني
- مسار تشريع الطلاق في العهدين المكي والمدني
- نداء الحق لامة الاسلام-فاعتبروا يا أولي الأبصار
- ضبط الخبر في اطار التفاوت في درجات الضبط والحفظ بي...
- الطلاق الشامل للدكتور عبد الغفار سليمان البنداري
- {10} الامرض المعدية
- {11}لجان الإشراف على أبحاث الخلايا الجذعية الجنيني...
- {12.} مؤسسة بيدفورد لأبحاث الخلايا الجذعية / معهد...
- متلازمة الإجهاد المزمن{المرض المزمن في الطفولة }
- أمراض المناعة الذاتية
- آزاثيوبرين{مضاد للالم ومثبط مناعي }{Azasan, Imuran}
- أمراض المناعة الذاتية للمحمول
- متلازمة الإجهاد المزمن {المرض المزمن في الطفولة }...
- مؤسسة بيدفورد لأبحاث الخلايا الجذعية البلد الولايا...
- لجان الإشراف على أبحاث الخلايا الجذعية الجنينية م ...
- الامرض المعدية {للمحمول}
- نسخة للمحمول الطلاق الشامل للدكتور عبد الغفار سلي...
- ضبط الخبر في اطار التفاوت في درجات الضبط{نسخة للمح...
- نداء سورة الطلاق نسخة للمحمول
- مسار تشريع الطلاق في العهدين المكي والمدني نسخة ...
- أسماء الله الحسني
- القائمة الرئيسية ***
- اقامة الشهادة للمحمول
- الزنجبيل فوائد طبية
- == سبانخ= السبانخ) فوائد طبية
- الكركم طبيا
- الاستجابات المناعية المتخصصة: الأجسام المضادَّة ال...
- وفاة النبي صلى الله عليه وسلم لأحمد بن شعيب النسا...
- قصة طباعة كتاب السنن الكبرى (سنن النسائي الكبرى)
- الإمام النسائي.. العلّامة المحدِّث صاحب السُّنن ال...
- الاستجابات المناعية المتخصصة: الأجسام المضادَّة ال...
- علاج سرطانات الجلد وغيرها سعفة ساقية تعفن سكر...
- العلماء ومسؤلياتهم الخطيرة علي ضياع دين الله في نف...
- ح الملحمة هيت ميل
-
▼
أغسطس 2023
(11)
******
لا تَقُومُ السَّاعَةُ حتَّى يَنْزِلَ الرُّومُ بالأعماق أو بدابق *******
الخميس، 7 سبتمبر 2023
ح الملحمة هيت ميل
<p style="text-align: center;"><a href="https://fadlll.blogspot.com/2023/11/blog-post_85.html"><span style="background-color: #fcff01;"><span style="font-family: Amiri; font-size: large;">لا تَقُومُ السَّاعَةُ حتَّى يَنْزِلَ الرُّومُ بالأعماق أو بدابق</span>
العلماء ومسؤلياتهم الخطيرة علي ضياع دين الله في نفوس المسلمين وقلوبهم وعقولهم// للمحمول
العلماء ومسؤلياتهم الخطيرة علي ضياع دين الله في نفوس المسلمين وقلوبهم وعقولهم
بإستقراء الأمور علي عقائدهم في واقعهم وقيام أعتي المواقع نصرة لدين الله تبين لي أن
.1أنهم وقفوا عند أول تقليد لأول تحريف للدين الحق في نفسه الضائع بين عاداتهم ونفوسهم هم في التقليد وتتبع الرجال دون رسول الله صلي الله عليه وسلم معرضين عن كتاب الله مضمونا وان سمحوا لتواجده بينهم شكلا
.2 أنشأوا بذورا للشيطان من الفرقة بينهم والتحزب ليزرع بها كفره بين عباد الله الغافلين ويروي بها شتلات ضلاله ويشبع بها نهم نفسه علي مر الازمان ما عدا أزمان الأنبياء وحوارييهم والصالحين المخلصين من عباد الله علي مر اوقاتهم
.3 وظل الأمر بين المسلمين ينمو علي ذلك ليحمل بذور الفساد التي زرعوها وأصلوا بها أعراف التقليد عازفين عن اتباع سبيل الهدي والرشاد من واقع قرانهم وحكمة نبيهم الكريم حتي تجدرت في الارض وترعرعت في الفضاء لكنها ترعرعت من معين أكثره باطل وقليله هو الحق حتي أسسوا لبناء كبير من الفرقة وطريقها لابعاد الناس عن اصول الحق السامية الثابته في كتاب الله وهدي نبيه صلي الله عليه وسلم
.4 وانعطفوا شمالا تاركين طريق ودرب الاستقامة بكل وضوح وبكل اصرار علي الانحراف شمالا حتي صار نور القران لا يؤثر فيهم وكلما ساروا تعمقوا في غيهم وفسادهم وابتعدوا شمالا وشمالا حتي انهم استمرؤوا ارتكاب كل الموبقات تحت مظلات المصطلحات التي صنعوها وأصبحوا لا يألفون السير بغيرها تلك المصطلحات التي حملت معاني التحريف والفواحش وكل الموبقات زاعمين أنها مغفورة مالم يأتوا شركا وتحصنوا بدروع صنعوها خصيصا لذلك الشأن وأصبح محمدا النبي الأكرم كأنه بعث لمجرد تقعيد قواعدهم بأن كل معاصيهم مغفورة من زني وسرقة وشرب للخمور وكل الغلول وكل ما يستجد من موبقات مالم يشركوا بالله بزعمهم وهم علي أهبة الاستعداد للمحاجة بقولم مذهب أهل السنة وتجأرهم أنه المذهب المعتدل الذي يشرع مالم يشرعه الله ورسوله مصدّْرين فهم للآية {{ إِنَّ اللَّهَ لَا يَغْفِرُ أَنْ يُشْرَكَ بِهِ وَيَغْفِرُ مَا دُونَ ذَلِكَ لِمَنْ يَشَاءُ وَمَنْ يُشْرِكْ بِاللَّهِ فَقَدِ افْتَرَى إِثْمًا عَظِيمًا (48)/ النساء}} والاية {إِنَّ اللَّهَ لَا يَغْفِرُ أَنْ يُشْرَكَ بِهِ وَيَغْفِرُ مَا دُونَ ذَلِكَ لِمَنْ يَشَاءُ وَمَنْ يُشْرِكْ بِاللَّهِ فَقَدْ ضَلَّ ضَلَالًا بَعِيدًا (116) إِنْ يَدْعُونَ مِنْ دُونِهِ إِلَّا إِنَاثًا وَإِنْ يَدْعُونَ إِلَّا شَيْطَانًا مَرِيدًا (117) لَعَنَهُ اللَّهُ وَقَالَ لَأَتَّخِذَنَّ مِنْ عِبَادِكَ نَصِيبًا مَفْرُوضًا (118) وَلَأُضِلَّنَّهُمْ وَلَأُمَنِّيَنَّهُمْ وَلَآمُرَنَّهُمْ فَلَيُبَتِّكُنَّ آذَانَ الْأَنْعَامِ وَلَآمُرَنَّهُمْ فَلَيُغَيِّرُنَّ خَلْقَ اللَّهِ وَمَنْ يَتَّخِذِ الشَّيْطَانَ وَلِيًّا مِنْ دُونِ اللَّهِ فَقَدْ خَسِرَ خُسْرَانًا مُبِينًا (119) يَعِدُهُمْ وَيُمَنِّيهِمْ وَمَا يَعِدُهُمُ الشَّيْطَانُ إِلَّا غُرُورًا (120) أُولَئِكَ مَأْوَاهُمْ جَهَنَّمُ وَلَا يَجِدُونَ عَنْهَا مَحِيصًا (121) /سورة النساء } وأباحوا بذلك الفهم المظلم حتي الانتحار وأخرجوا كل اصحاب الكبائر بمن فيهم المنتحرين تعمدا وقتلة النفس التي حرم الله الا بالحق والميتين مصرين علي ذنوبهم وأقحموهم علي الله الواحد جبرا بسفاهتهم سبحانه وهو لا يجبر ولا يقهر بدعوي أنهم اي اولئك المصرين علي أباطيلهم من الموحدين وقلت في نفسي هل هناك موحدين مصرين علي عصيان الله لدرجة الموت علي عصيانهم وكتشفت أنهم أهل السنة فقلت في نفسي ان كان حال اهل السنة هكذا واليهم يذهب الهدي فما بال من يجهلون وبدينهم لا يعلمون لكني تبينت أن أهل السنة هم حملة تراث النووي ومحرفوا النصوص بتجأر لم أر له شبه ولا مثيل
ويستكمل ان شاء الله اتيا
علاج سرطانات الجلد وغيرها سعفة ساقية تعفن سكروت{للمحمول}
مراجع ومنقح جدا علاج سرطانات الجلد وغيرها
سعفة ساقية
تعفن سكروت
معلومات عامة
الاختصاص أمراض معدية
من أنواع قوباء حلقية، ومرض جلدي
أدوية{{ سولكونازول، ولوليكونازولي،
وأوكسيكونازول
----------------------
السعفة الساقية أو
سعفة الفخذ أو سعفة باطن الفخذين والمغبن أو سعفة الأرفاغ أو تعفن سكروت
(باللاتينية: Tinea cruris) (بالإنكليزية البريطانية) أو حكة جوك (بالإنجليزية: jock itch) (بالإنكليزية الأمريكية) هي عبارة عن عدوى فطرية للمنطقة
العجانية عند الذكور والإناث
،
ولكنها تكون أكثر شيوعاً عند الرجال منها عند النساء.
الأعراض
و كما يدل اسم المرض فإن الأعراض
تظهر على شكل حكة وشعور بالحرقة في المنطقة الحنية ومنطقة طيات الجلد الفخذية
والشرجية. كما يمكن أن تمتد إلى المنطقة الداخلية من الفخذ وإلى الأعضاء التناسلية
وإلى كل من المنطقة العجانية وحول الشرجية.
تتلون المناطق المصابة بالحمرة أو
السمرة أو تكون مائلة للون البني ويكون الجلد متشقق ومجعد ويميل إلى التقشر ثم
التساقط.تبدأ العدوى في الطور الحاد من طيات المنطقة الحنية بحجم نصف انش، وغالباً
ما تكون على الجانبين، ثم تكبر وتمتد إلى مناطق أخرى من غير شكل مميز. تظهر
الأعراض على شكل بقع محمرة مرتفعة وبقع متقشرة مع حدود مرتفعة مميزة.
عندما تتطور الأفة فقد تمتد إلى
الأسفل باتجاه منطقة الفخذ الداخلية. تكون الحواف المتقدمة أكثر حمرة وارتفاعاً من
المناطق المخموجة والتي مضى عليها وقت أطول. تكون الحواف المتقدمة متقشرة ومميزة
بشكل واضح.
العامل المسبب
تنتج هذه الإصابة من العدوى
الانتهازية على الأغلب. حيث أن بعض الفطور من مناطق أخرى من الجسم (مثل قدم
الرياضي) يمكن أن تتسبب بهذه الإصابة. تؤمن المناطق الحارة والرطبة جواً مناسباً لتكاثر
الفطور وخاصة عند لبس الملابس الضيقة وحدوث احتكاك شديد مع الجسم. أغلب الفطور
شيوعاً في التسبب بهذه الإصابة هو فطر تريكوفايتون روبروم. كما يمكن للمبيضات
البيض أن تلعب دوراً في الإصابة.
الوقاية
ينصح الأطباء
بالوقاية لمنع الفطريات من التكون حتى لا تقع تعفن سكروت. الوقاية تكون بإزالة
الحرارة والرطوبة من منطقة الفخذين.تنشيف المنطقة بفوطة نظيفة بعد الانتهاء من
الأستحمام أو السباحة أو التعرق.
تنشيف بعد الأنشطة البدنية.
لبس ملابس داخلية كتانية لأن ليدهم
منع قوي للهواء والرطوبة.
تجنب ملابس البوليستر لأنها تساعد
على تكوين الفطريات والبكتيريا.
العلاج
أفضل علاج لتعفن سكروت هو المضادات الفطرية بنوع allylamine أو azole ،
= وأيضا التي تحتوي على تيربينافين ونافتيفين
اقرأ أيضاً القوباء الحلقية
المضاد الفطري
==============
فطريات جلدية
الفطور الجلدية (باللاتينية: Dermatophytes) هي فطريات طفيلية تهاجم
الجلد. تتضمن هذه المجموعة ثلاثة أجناس من الفطريات غير الكاملة وهي الشعروية،
مايكروسبورم Microsporum، إبيديرموفايتون Epidermophyton. هذه
الأجناس الثلاثة هي عبارة عن أطوار غير جنسية ويتبع لها ما يقارب 40 نوع. أما الأنواع
القادرة على التكاثر الجنسي فإنها تتبع للجنسين التاليين: أرثروديرما Arthroderma والفطريات الزقية.
تسبب الفطور الجلدية عدوى للشعر والجلد والأظافر نظراً
لقدرتها على التغذية على المواد الكيراتنية. حيث تشكل هذه الفطريات مستعمراتها في
الأنسجة الكيراتينية ومن ثم يحدث الالتهاب كرد فعل للجسم على نواتج الاستقلاب
الثانوية للفطريات. وبشكل عام ينحصر تواجد هذه الفطريات على الطبقة المتقرنة من
البشرة وذلك لعدم قدرتها على اختراق الأنسجة الحية في جسم المضيف ذو المناعة
السليمة. تستجر هذه العدوى استجابة مناعية من الجسم المضيف تتراوح من معتدلة إلى
شديدة. كما وتلعب كل من الأنزيمات التالية: بروتينيز، إيلاستيز، كيراتينيز، وغيرها
من الأنزيمات المحللة للبروتينات دوراً في ضراوة هذه الفطريات. هذا وإن تطور الجسم
المضيف لمناعة خلوية مرتبطة مع فرط التحسس المتأخر من شأنه أن يساعد على الشفاء
على عكس المضيفون الذين يعانون من مشاكل في مناعتهم الخلوية ومما يمهد لعدوى فطرية
مزمنة أو متكررة.
يطلق عادة على العدوى المسببة بالفطريات الجلدية اسم
القوباء الحلقية أو بشكل أدق تينيا
Tinea.عادة لا تغزو هذه الفطريات الأنسجة الحية بل
الطبقة الخارجية من الجلد وفي حالات نادرة تغزو الأنسجة تحت الجلدية مسببة تشكل
الكريون kerion.
أنواعهاقدم الرياضي أو سعفة القدم Tinea pedis
تصيب الرجال أكثر من النساء وهي إصابة غير محصورة فقط
على الرياضيين كما يوحي الاسم بذلك. تبدأ الإصابة في الفراغ بين الأصابع الأولى
للقدم ومن ثم يمتد إلى باطن القدم على شكل الحذاء المنزوع الكعب. حكة جوك Tinea cruris
تصيب هذه الحكة بشكل رئيسي المنطقة الحنية ومن ثم تنتشر
إلى مناطق أخرى من الجسم مثل المنطقة الحول شرجية ومنطقة الإلية. تحدث العدوى عادة
بانتقال الأبواغ إلى المنطقة الحنية بواسطة الحك. القوباء الحلقية المنتشرة في
كامل الجسم أو سعفة الجسم Tinea
corpora
القوباء الحلقية في الوجه أو سعفة الوجه Tinea faciei
القوباء الحلقية المسببة للنقط السوداء أو سعفة الرأس Tinea capitis
تتميز هذه الإصابة بتكسر ساق الشعرات المصابة من جذورها
تاركة ورائها نقاط سوداء على الجلد. كما تعتبر الكشطات المأخوذة من منطقة النقط
السوداء أداة تشخيصية هامة عند استخدام المجهر. يظهر الفحص المجهري تواجد أبواغ
متعددة من نوع أرثروسبوز.لا تتم معالجة هذه العدوى موضعياً وإنما بالمعالجة
الجهازية بمضادات الفطور.القوباء الحلقية في فروة الرأس Tinea capitis
القوباء الحلقية في اليدين أو سعفة اليدين Tinea manuum
غالباً ما تحدث الإصابة في يد واحدة وفي كلتا القدمين.
عدوى الأظافر الفطرية
Onychomycosis أو سعفة الأظافر Tinea unguum
التشخيص
يمكن أن يتم التشخيص بسهولة بأخذ كشطات من الأظافر أو
الأشعار أو فروة الرأس حيث تظهر خيوط فطرية مميزة متناثرة بين الخلايا الظهارية.
كما يتم اللجوء إلى منابت فطرية للعزل الإيجابي لأنواع
الفطور. تحتاج الفطور عادة فترة تتراوح بين 5-14 يوم للنمو في المنابت. يعد
التمييز المجهري للأبواغ الكبيرة والصغيرة من الإجراءات المعتمدة في التفريق بين
الفطور. ولكن هذه العملية تحتاج إلى مستعمرات محضرة بشكل جيد على الشريحة الزجاجية
وإلى تحريض على التبوغ في العديد من الأنواع. من ناحية أخرى فإن الخصائص الشكلية
للمستعمرة من ناحية نوع النسيج الفطري والتصبغ والتضاريس هي أيضاً مهمة في
التشخيص. كما أنه من الأهمية بمكان الإحاطة بالمعلومات السريرية للحالة من ناحية
مكان الإصابة وانتشارها وتاريخ السفر أو الاحتكاك بالحيوانات وخاصة في حالة
الأنواع التي ليس لها القدرة على تشكيل أبواغ مثل Trichophyton
concentricum, Microsporum audouinii، Trichophyton.schoenleinii
و لقد تم تطوير منبت خاص يدعى منبت فحص الفطور الجلدية (DTM) من أجل
تشخيصها والذي يعتمد على تلون المنبت من اللون الأصفر إلى الأحمر عند تواجد أحد
أنواع هذه الفطريات دون الحاجة للتشخيص المجهري.
حيث يتم غرس العينات السريرية بهذا المنبت ومن ثم
تحضينها على درحة حرارة الغرفة لمدة 10-14 يوم لملاحظة التغير اللوني. بعد أسبوعين
من التحضين قد تظهر نتائج كاذبة لذلك يجب أن لا تتجاوز المدة 14 يوماً.
الانتقال
تنتقل الفطور الجلدية من خلال الاتصال المباشر أو غير
المباشر مع المضيف المصاب (حيوان أو إنسان). حيث يتم من خلال التماس مع الجلد أو الشعر أو
حتى الملابس أو أمشاط الشعر أو المقاعد أو المناشف أو سجاد الفنادق أو أرضية غرف
تبديل الملابس. يمكن لهذه الفطريات أن تبقى حيوية في البيئة حتى 15 شهراً وذلك حسب
الأنواع. كما تعد الإصابات الجلدية منل الحروق والجروح من العوامل المساعدة على
الإصابة بالإضافة إلى الحرارة والرطوبة.
التصنيف
تصنف الفطور الجلدية بناءً على أماكنها المحببة للتعايش
إلى ثلاثة مجموعات: المحبة للإنسان: تنحصر الإصابة عند الإنسان وهي تظهر عدوى
متوسطة ممزمنة.
المحبة للحيوان: وهي تتواجد بشكل رئيسي عند الحيوانات
ولكن من الممكن أن تنتقل إلى الإنسان عند الاتصال مع حيوان مصاب.
المحبة للتربة: تتواجد في التربة ولكنها ممن الممكن أن
تصيب الإنسان والحيوان.
العلاج
العلاج الموضعي بأحد المركبات التالية:clotrimazole, miconizole, terbinafine
العلاج الجهازي يتم عن طريق الفم مثل: fluconizole, griseofulvin, Terbinafine,
itraconizole.
وصلات خارجيةعالم الفطريات الجلدية (بالإنجليزية)
المراجع
=======
سعفة القدم
سعفة القدم
معلومات عامة
الاختصاص أمراض معدية
من أنواع قوباء حلقية، ومرض القدم، ومرض جلدي، ومرض
الإدارة
أدوية
ميكونازول، ونافتيفين، وإيكونازول، وسيكلوبيروكس،
وبوتينافين، وأوكسيكونازول، وغريسيوفولفين، وكيتوكونازول، وتيربينافين،
وهالوبروجين، وتولنافتات، وهيبوكلوريت الصوديوم، وسولكونازول، وسولكونازول،
ولوليكونازولي، وأوكسيكونازول
تعديل مصدري - تعديل

tinea pedis أو قدم الرياضي
سعفة القدم أو القدم الرياضي (بالإنجليزية: Athlete's foot) هو مرض فطري يصيب الجلد، يتعرض
الرياضيون أكثر من غيرهم للإصابة به؛ لأن أقدامهم أكثر من غيرهم عرضة لارتفاع درجة
حرارتها وزيادة رطوبتها بسبب الأحذية الرياضية والتدريب، وفطريات قدم الرياضي
معدية على نحو كبير، وتنتقل إلى الآخرين إذا مشى المصاب حافيَ القدمين على أرض حوض
السباحة أو غرف تغيير الملابس، أو تشارك في استعمال المناشف أو أحذية الرياضية.
ويمكن أن تنتشر الإصابة أيضاً إلى أجزاء أخرى من الجسم، مثل الاظافر
الأعراض
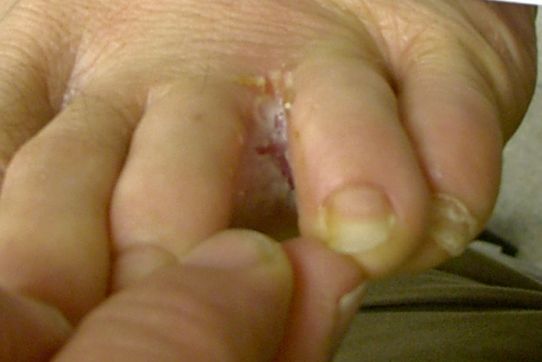
تسلخ الجلد بين
الأصابع
يتسبب هذا المرض بإحداث تقشر وتساقط مع حكة للجلد في
المنطقة المصابة. كما يمكن أن يتشقق الجلد وتظهر بثرات مما يؤدي إلى ظهور الأنسجة
الداخلية مع ألم وانتفاخ والتهابات. وغالباً ما تترافق هذه العدوى الفطرية بعدوى
جرثومية ثانوية الأمرالذي يتطلب استخدام المضادات الحيوية. يمكن أن تنتشر العدوى
إلى أماكن أخرى من الجسم مثل منطقة العجان وعندئذ تسمى العدوى بمسميات مختلفة
بناءً على مكان العدوى كما هو الحال في القوباء الحلقية. غالباً ما يكون مكان هذه
الإصابة بين أصابع القدم وخصوصاً بين الإصبعين الرابع والخامس.
التشخيصيتمكن أن يتم التشخيص إما من قبل الصيدلي أو الطب
العام أو حتى أخصائيي الجلد وإصابات الأقدام. تشخص هذه العدوى غالباً بالعين
المجردة وفي حالات الشك يتم اللجوء إلى المجهر الضوئي بعد معالجة العينات
بهدروكسيد البوتاسيوم KOH وتدعى هذه المعالجة ب اختبار هيدروكسيد البوتاسيوم. يساعد
التشخيص باستخدام المجهر الضوئي على استبعاد حالات الإكزيمة والصداف والتي تشابه
بأعراضها عدوى قدم الرياضيين. يعتبر اختبار هيدروكسيد البوتاسيوم ذو قيمة عالية في
تشخيص مثل هذه الحالات ولكن لسوء الحظ ممكن أن يعطي نتائج خاطئة وخاصة عند البدء
باستخدام مضادات الفطور قبل التشخيص.
في مثل هذه الحالات يتم اللجوء إلى التشخيص النسيجي
بالاعتماد على خزعات من الجلد المصاب.
انتقال العدوى
من شخص لآخرتتسبب هذه الإصابة بفطريات طفيلية وهو مرض
مرض قابل للانتقال. ينتقل هذه العدوى بشكل نموذجي في البيئات الرطبة وعند المشي
بشكل حافي مثل الحمامات وخزائن تبديل الملابس
ومواضيء المساجد. كما يمكن أن ينتقل المرض عند الاستخدام
المشترك للأحذية والشباشب وبشكل أقل عند الاستخدام المشترك للفوط. وحذار من انتقال
السعفة من القدم إلى أماكن أخرى من الجسم، مثل الأعضاء التناسلية. فيجب علاجها
بالمراهم والاهتمام بنظافة اليدين بعد الاستعمال.
إلى أماكن أخرى من الجسم
يمكن أن تتنتشر هذه الفطريات الطفيلية التي تسبب قدم
الرياضي إلى مناطق أخرى من الجسم وخاصة أظافر أصابع القدم وتسبب ما يعرف ب Onychomycosis أو
المنطقة الحنية tinea cruris.
الوقاية
تساعد الإجراءات الوقائية ليس فقط في تجنب الإصابة عند
الإنسان السليم بل أيضاً في شفاء المرضى من خلال عدم التعرض المتكرر للعامل
المسبب. مع علمنا المسبق بأن هذه الفطريات تعيش في المناطق الرطبة مثل الحمامات
وغرف تبديل الملابس ومواضيء المساجد حيث يتبادل المصلون الأحذية المبللة عند
الوضوء . فيجب الحفاظ على الأرجل جافة ونظيفة قدر الإمكان والوضوء بالمنزل .
بالإضافة لذلك فإن العناية الصحية العامة تلعب دوراً هاماً في الوقاية كأن لا يتم
استخدام الفوط والأحذية بشكل مشترك وبالتالي تقليل فرص التعرض للعوامل المؤدية
لمثل هذه الحالات.
العلاجلقد أظهرت الدراسات بأن حوالي 30-40% من الحالات
تشفى بمجرد أخذ إجراءات الصحة العامة. كما يتم العلاج باستخدام مركبات الآزول حيث
يحقق الأخير نسبة شفاء أعلى.
تباع مراهم في الصيدليات صنعت خصيصا لمعالجة تلك
الفطريات، كما يمكن السؤال في الصيدلية عن الاستخدام الأمثل لتلك المراهم إذ يوجد
منها أنواع عديدة.
=========
مضادات الفطريات
المضادات الفطرية (بالإنجليزية: Antifungal drugs)
هي أدوية تستخدم في
علاج الإصابات الفطرية مثل مرض قدم الرياضي ومرض القوباء الحلقية بالإضافة للعدوى
بالمبيضات البيض والعدوى الفطرية الجهازية.
لقد كان للانتشار المروع لكل من عدوى النسوجيات وعدوى
الكورانية في نهاية القرن التاسع عشر الأثر الأكبر في دفع الجهود باتجاه إيجاد
دواء فعال لعلاج تلك العدوى الخطيرة والقاتلة. لكن لسوء الحظ فلم تتكلل هذه الجهود
بالنجاح حتى 1960 وذلك بالتوصل إلى كل من النيستاتين والأمفوتيريسين ب والفيليبين
والهامايسين.
تعدّ التطورات الحاصلة على المستوى الطبي في مجال علاج
السرطان وزرع الأعضاء بالإضافة إلى الوقاية المتبعة عند الإصابة بالإيدز هي
المسؤولة عن الارتفاع الخطير في معدل إصابة الأشخاص بخلل في جهاز المناعة مما
يجعلهم عرضة لعدوى فطرية قد تهدد حياتهم. وبناءً عليه فقد تم العمل الجاد لإيجاد
طرق جديدة لعلاج هكذا عدوى تتجاوز بفعاليتها الطرق التقليدية في العلاج.
نبذة تاريخية
في ستينيات القرن الماضي تم التوصل إلى اكتشاف كل من
النستاتين والأمفيتراسين ب والفيليبين والهامايسين كمضادات فطرية ولكن بسبب سميتها
فقد تم استبعاد الفيليبين وأبقى على استخدام النستاتين والهامايسين للاستخدام
الموضعي وعلى الأمفيتراسين ب للعلاج الجهازي.
كما تم التوصل أيضاً إلى اكتشاف فلوسايتوسين ذو التأثير
الفعال على كل من المبيضات والرشاشيات. حالياً يتم استخدامه فقط مع الأمفيتراسين ب.
ومن ثم تم اكتشاف مركبات الآزول والتي تعدّ حقبة جديدة
في تاريخ المضادات الفطرية من حيث فعاليتها وسميتها الخفيفة. أول هذه المركبات كان
كلوتريمازول الذي اكتشف لاحقاً بأنه يسبب أضرار عند اعطائه بشكل جهازي واقتصر
استخدامه على العلاج الموضعي. أما المركب الثاني فهو مايكونازول وقد تم استخدامه
حقناً عن طريق الوريد لسنوات عديدة قبل أن يكتشف تأثيره الضار وتحوله إلى دواء
للاستخدام الموضعي. ثم تم اكتشاف كيتانونازول حيث اعتبر مرحلة جديدة في عمر هذه
المركبات حيث تتمتع بفعالية دوائية ذات طيف واسع في علاج الفطريات عند استخدامه عن
طريق الفم. في ثمانيات القرن الماضي تم التوصل إلى
فلوكونازول
وإتراكونازول.
خلال فترة تطور
مركبات الآزول كان العمل جارياً على تعديل الأمفيتراسين ب لزيادة فعاليه والتخفيف
من تأثيره السمي وأفضل ما تم التوصل إليه في هذا المجال كان بدمج جزيئات هذه
الدواء مع حوامل دهنية.
مضادات الفطور التقليدية
1- مضادات الفطور الببتدية (بالإنجليزية: Antifungal Peptides)
تختلف هذه المركبات في تأثيرها ولكن بشكل عام تعمل هذه
المركبات على قتل أو تثبيط النمو عند الفطور من خلال تحليل أو الاقتران أو تخريب
الغشاء السيتوبلازمي وتشكيل ثقوب فيه ومن ثم حدوث تسرب في المحتويات الخلوية أو من
خلال تأثيرها على السيتوبلازما أو النواة. تكون مضادات الفطور الببتدية الطبيعية
مشتقة إما من:
الجراثيم (إتيورين (بالإنجليزية: Iturin)،
= باسيلومايسين
(بالإنجليزية: Bacillomycin)، = = سيرينجوتوكسين (بالإنجليزية:
Syringiotoxins)،
=سيباسيدين (بالإنجليزية:
Cepacidines))
=الفطور (إتشينوكاندين (بالإنجليزية: Echinocandins))
الحشرات (سيسروبين أ، ب Cecropins A and B، دورسومايسين (بالإنجليزية: Drosomycin)،
= ديرماسنتين
(بالإنجليزية: Dermaseptin))
النباتات (زيماتين (بالإنجليزية: Zeamatin)، فرانجفلولين (بالإنجليزية: Frangufloline)، نومميولارين (بالإنجليزية: Nummularine))
الثدييات (جالنسين (بالإنجليزية: Gallinacin)).
2- مضادات الفطور المانعة لتشكيل الكيتين (بالإنجليزية: Chitin Synthase Inhibitors)
يتواجد الكيتين في الغشاء السيتوبلامي الخلوي ويعد غيابه
من جدران الخلايا عند الثدييات هدفاً محتملاً من أهداف الاستراتجيات الدوائية
المتبعة في معالجة الفطور. من أم المركبات التي تعمل على تثبيط تركيب الكيتين هي:
نيكومايسين (بالإنجليزية:
Nikkomycin)
وبولي أوكسين (بالإنجليزية:
Polyoxins).
3- مضادات الفطور التي تستهدف الغشاء السيتوبلازمي أو
الاستقلاب
أ)- البولين (بالإنجليزية: Polyenes)
تتحد مركبات هذه المجموعة بسرعة مع المركبات الستيرولية
(بالإنجليزية: Sterol) وبشكل محبب
الأرجيستيرول (بالإنجليزية:
Ergosterol)،
الذي يشكل الستيرول الرئيسي في تركيب غشاء الخلية الفطرية. بينما تتحد بشكل أقل
حدة مع الكولسترول، المكون الستيرولي الرئيس في جدارن الخلايا عند الثدييات. كنتيجة لهذا
الاتحاد يحدث تخريب لجدران الخلايا مع حدوث تسرب للبوتاسيوم والمغنيزيوم
المتواجدان داخل الخلايا ومن ثم موت الخلية الفطرية. من جهة أخرى تخرب هذه
المركبات الأنزيمات المسؤولة عن عملية الأكسدة في الخلايا المستهدفة وبالتالي موت
الخلايا. تتضمن هذه المجموعة مركبات تستخدم بشكل شائع في علاج العدوى الفطرية:
نيستاتين (بالإنجليزية: Nystatin): يستخدم للعلاج
الموضعي على شكل معلق يؤخذ عن طريق الفم.
أمفوتيراسين ب (بالإنجليزية: Amphotericin B): يستخدم للعلاج الجهازي عن طريق الحقن بالوريد ويتواجد تحت عدة
أسماء تجارية.
SPA-S-753 (ن ميثيلأمينوأستيل-بارترسين أ2
ديمثيلأمينوإثيلأميد ديسوربيت)
(N-dimethylaminoacetyl-partricin A2-dimethyl-aminoethylamide diascorbate)
ب)- الآزول (بالإنجليزية: Azoles)
تعمل هذه المركبات على تثبيط السايتوكروم عند الفطور،
ديميثيليز الموسوم س14. حيث أن تثبيط هذا الإنزايم يؤدي إلى منع تشكل الأرجوستيرول
من أجل جدار الخلية الفطرية. أيضاً يتم تعطيل أنزيمات الأكسدة المترافقة مع الغشاء الخلوي
بالإضافة إلى تجمع الدهون الفوسفورية ضمن الخلية وبالتالي موتها. تقسم هذه
المجموعة كيميائياً إلى مجموعتين: إميدازول (بالإنجليزية: Imidazoles): تتضمن كلوتريمازول (بالإنجليزية: Clotrimazole)، إيكونازول (بالإنجليزية: Econazole)، كيتوكونازول (بالإنجليزية: Ketoconazole)، مايكونازول (بالإنجليزية:
Miconazole).
تريآزول (بالإنجليزية: Triazoles): تتضمن فلوكونازول (بالإنجليزية: Fluconazole)، إتراكونازول (بالإنجليزية: Itraconazole)، تيركونازول (بالإنجليزية: Terconazole)، أمورولفين (بالإنجليزية:
Amorolfine).
===========
الباب الثاني
علاج السرطان والأمراض الجلدية التي لها ظهور علي الجلد بالكي المائي المغلي جداً.
دكتور عبد الغفار سليمان البنداري
بسم الله الرحمن الرحيم ، والحمد لله رب العالمين،وأشهد أن لاإله إلا الله ولي الصالحين،وأشهد أن محمداً رسول الله إلي الناس أجمعين،والصلاة والسلام علي المبعوث رحمة للعالمين، أما بعد فهذا البحث قد أجريته في البريفت الخاص بي علي مجموعة معتبرة من المرضي ،حيث تأصل علي الأساس العلمي المشابه لما كان عليه تطعيم الجدري سابقا،وكان تطعيم الجدري فيما مضي يقوم علي لصق الأجسام المضادة الميتة أو المضعفة علي طبقة الجلد الموجودة بأعلي العضد من الذراع الشمال ، وكان الغرض من التطعيم الذي أثبت جدارة عالية جداً هو أن يقوم جهاز المناعة النوعي الخاص بالشخص بالتعرف علي الفيروس الملصق علي الجلد وهو في أضعف أحوال الفيروس ،والغرض من هذا أن تبدأ العملية المناعية الخلوية والهيوميرالية علي التوازي بما ينتج في محصلة هذا الميكانيزم مناعة صارمة ممتدة لا تنحدر مع الأيام ولا تضعف أمام شدة وقوة الفيروسات الجدرية،إذن كيف ﻳﺘﻢ إﻋﻄﺎء اﻟﻠﻘﺎح علي سطح الجلد فيما مضي وكيف نطعم مريض السرطان الذي لسرطانه ظهور علي مسطح الجلد أو ذو الأفة الجلدية لكي ننشأ عنده مناعة دائمة ضد المرض ؟
1-💥 نموذج التطعيم ضد الجدري
^ كان فيما مضي ﻳﺘﻢ إﻋﻄﺎء ﻟﻘﺎح اﻟﺠﺪري ﺑﺎﺳﺘﺨﺪام إﺑﺮة ﺛﻨﺎﺋﻴﺔ اﻷﻃﺮاف(ولا ﻳﺘﻢ إﻋﻄﺎء ﻟﻘﺎح اﻟﺠﺪري ﺑﺈﺑﺮة ﻋﺎدﻳﺔ)
^ حيث ﻳﺘﻢ إﻋﻄﺎء اﻟﻠﻘﺎح بغمرها ﻓﻲ ﻣﺤﻠﻮل اﻟﻠﻘﺎح، وﻋﻨﺪ إﺧﺮاﺟﻬﺎ ﻣﻦ اﻟﻤﺤﻠﻮل ﺗﺤﺘﻔﻆ اﻹﺑﺮة ﺑﻘﻄﺮة ﻣﻦ اﻟﻠﻘﺎح
^ﻳﺘﻢ اﺳﺘﺨﺪام اﻹﺑﺮة ﺑﻌﺪ ذﻟﻚ ﻟﻮﺧﺰ اﻟﺠﻠﺪ ﻋﺪة ﻣﺮات ﺧﻼل ﻋﺪة ﺛﻮان. ﻻ ﻳﻜﻮن اﻟﻮﺧﺰ ﻋﻤﻴﻘﺎ،ويكون سطحياً أي تحت الجلد(subcutenious) وﻟﻜﻨﻪ ﺳﻴﺘﺴﺒﺐ ﻓﻲ أن ﻳﻜﻮن هناك ﺟﺰءٌ ﻣﺆﻟﻢٌ وﻗﺪ ﺗﺘﻜﻮن ﻗﻄﺮة أوﻗﻄﺮﺗﺎن ﻣﻦ اﻟﺪم.
^كان ﻳﺘﻢ إﻋﻄﺎء اﻟﻠﻘﺎح ﻋﺎدة ﻓﻲ أﻋﻠﻰ اﻟﺬراع.
^ فإذا كان اﻟﺘﻄﻌﻴﻢ ﻧﺎﺟﺤﺎ ﻳﻈﻬﺮ ﻧﺘﻮء أﺣﻤﺮ وﻣﺜﻴﺮ ﻟﻠﺤﻚ ﻓﻲ اﻟﻤﻨﻄﻘﺔ اﻟﺘﻲ ﺗﻢ ﺑﻬﺎ اﻟﺘﻄﻌﻴﻢ ﺧﻼل ﺛﻼﺛﺔ أو أرﺑﻌﺔ أﻳﺎم. وﻓﻲ اﻷﺳﺒﻮع،اﻷول ﺑﻌﺪ اﻟﺘﻄﻌﻴﻢ ﻳﺼﺒﺢ اﻟﻨﺘﻮء ﺑﺜﺮة كبيرة وﺗﻤﺘﻠﺊ ﺑﺎﻟﻘﻴﺢ وﺗﺒﺪأ ﻓﻲ اﻟﺘﺴﺮﻳﺐ.
^أﺛﻨﺎء اﻷﺳﺒﻮع اﻟﺜﺎﻧﻲ ﺗﺒﺪأ اﻟﺒﺜﺮة ﻓﻲ اﻟﺠﻔﺎف وﺗﺘﻜﻮنﻗﺸﺮة.
^حيث ﺗﺴﻘﻂ اﻟﻘﺸﺮة ﻓﻲ اﻷﺳﺒﻮع اﻟﺜﺎﻟﺚ ﻣﺨﻠﻔﺔ وراﺋﻬﺎ ﻧﺪﺑﺔ. وكانت الوقاية تتم وذلك باستخدام فاكسين أو لقاح الجديري المائيVaricella Vaccine. حيث كان يعطي حماية من الإصابة بالمرض بنسبة 90% تقريبا(وذلك ضمن برنامج اليونيسيف التطعيمي للأطفال )،
= ولايجدي تعاطيه فى وقت الإصابة ^الأطفال: كانت الأطفال تعطي جرعتان من اللقاح.
الجرعة الأولى في سن 12-15 شهر.
والجرعة الثانية في سن 4-6 سنوات.
و إذا لم يأخذ الطفل اللقاح في هذا السن فإنه يمكن أن يأخذه في سن 7-12 سنة.
ويكون في صورة جرعتين منفصلتين بين الجرعة و التي تليها على الأقل 3 شهور.
والأطفال الأكبر من 13 عاما الذين لم يأخذوا اللقاح من قبل يمكن إعطاء اللقاح لهم في صورة جرعتين يفصل بينهما على الأقل 4 أسابيع.
٢-💥 أما البالغين :فكان يمكن للبالغين الذين لم يأخذوا اللقاح في مرحلة الطفولة أن يتم أخذ اللقاح إذا كان هناك خطورة للإصابة بالجديري المائي.
وكان يتم إعطاء اللقاح في صورة جرعتين يفصل بينهما 4-8 أسابيع على الأقل]،
٣-💥
كيف يتم ذلك علي الجلد بطريق الكي الرطب؟ في علاج السرطانات التي لها ظهور علي الجلد والامراض الفطرية والبكتيرية الجلدية المزمنة والامراض المناعية الذاتية
قلت المدون
وبمثل هذا التيكنيك،أو بقريب منه يتم تطعيم المريض بالسرطان بالخلايا السرطانية الذاتية المضعفة أو المقتولة،أو بخلايا الأمراض الجلدية التي لها ظهور علي الجلد وإلصاقها بالجلد عن طريق الكي الرطب؟
ولكن كيف يتم لصق وتثبيت الخلايا الميتة السرطانية،أو أي خلايا مرضية أخري لها ظهور علي الجلد كالتينيا،والصدفية،واللوبس إريزيماتوزس،والإكزيما،والجرب الجلدي،البهاق، وغير ذلك من الأمراض المزمنة و التي لها ظهور علي الجلد ومنها بالطبع الخلايا السرطانية المتواجدة علي الجلد؟
الخطوات العملية:
1 - يتم اختيار منطقة تواجد مكثف نسبيا للمرض علي الجلد،تكون في الإصابات الجلدية كالتينيا والإكزيما والصدفية(بعد تقشير الصدفات القشرية وتعرية ما تحت الصدفات من جلد في هذا البقعة[لا تزيد علي دائرة قطرها حوالي 10-15سنتيمترا مربعا علي سطح الجلد]،أو منطقة القرحة السرطانية المتواجدة علي العضو(مثل قرحة الثدي السرطانية، أوقرحة الفم السرطانية، أو أي قرحة سرطانية لها ظهور علي الجلد،
2- تعقم البقعة الجلدية من البكتيريا المتواجدة بسطحها تعقيما جيدا بمطهر كالكحول فإن كانت القرحة السرطانية فيمكن استخدام مطهر بكتيريٍ آخر مثل البيتادين أو ماء الأكسجين.
3- تغمس قطعة شاش مطوية ممسوكة بجفت غيار أو جفت شرياني،في ماء مغلي لدرجة الغليان القصوي ثم توضع مباشرة علي البقعة الجلدية التي سبق تحديدها، حتي تخبو حرارتها ،ثم تكرر هذه الطريقة مرة أخري أو مرتين حتي يتأكد للطبيب حدوث حرق من الدرجة الأولي مهيأ لتكوين فقيعة مائية(Bulous) بعد عدة ساعات من مبادرة الحرق المائي (ملحوظة:يجب أن تحرص علي تكون هذه البوللاس المائية(BULLOUS)بدون فقع(RupturING)لها لأن تفاعل المناعة سيحدث في هذا الوسط بين خلايا الجهاز المناعي الخلوي والهيوميرالي(الخليط)،من ناحية وبين الأنتيجين من الناحية الأخري(ملحوظة: معني الأنتيجين هو الفيروس أو الفطريات الجلدية الباثوجينية أو الخلايا الممنعة ذاتيا للأمراض مجهولة الهوية والسبب أو الخلايا السرطانية فإن كل هذه تسمي أنتيجينات).
4.نقوم بتثبيت الأنتيجين المقتول والمضعف نتيجة تهالكه في بيئة الحريق الذي أحدثناها علي البقعة المصابة نتيجة عملية الكي المائي الحارق وفيها الفيروس أو الخلايا المرضية التي تحتوي علي كسرات الفيروس الشفرية أو الأنتيجين المضعف المقتول بالكي المائي الحارق وله خاصيته الشفرية:(Antigenic)DIED Or Weakened Fragmentes) ،وذلك بتغطية الجلد المكوي مائياً برباطٍ من الشاش المعقم و المفزلن في آن واحد حتي يتسني للجرح التفاعل المناعي كما سيرد شرحه تفصيليا هنا بإذن الله تعالي.
5.يترك الجرح ثلاثة أيام مغطي بالشاش بغير فتح،حتي يتكون تفاعل صديدي محدود،ويحدث ألماً نسبياً بالجزء المكوي وتكون حرارة المريض لا تزيد علي 37.5 أو38 درجة مئوية،بحيث لو زادت علي ذلك نلجأ إلي منح المريض مضاداً حيوياً بكتيريا لمعالجة ما يمكن أن يتسرب من نموٍ بكتيريٍ ثانويٍ علي الجرح(الحرق المائي بالجلد)،مع ضرورة إبقائنا علي الشاشة المثبتة علي سطح الجلد والرازحة علي الأنتيجين الذي تم قتله،أو تضعيفه في مكان الجلد المكوي بالماء المغلي،
6.يرفع الغطاء الشاشي(الشاشة المثبتة علي الجلد المكوي)عند مظنة التئام الجرح(عادة يلتئم الجرح المكوي بعد اسبوع أو عشرة أيام من الكي ،ثم يترك المريض ثلاثة أسابيع حرا من غير كي آخر،ثم يكرر التطعيم مرة أخري بهذه الطريق،وفي حالة الإصابة السرطانية يكرر التطعيم بهذه الطريقة للمرة الثالثة بعد ثلاثة أسابع أخري، ثم بعد شهرين،ثم بعد ثلاثة أشهر فيكون مجموع التطعيمات بالكي لمريض السرطان خمسة تطعيمات.
ولكن ما الذي يتم عند حدوث هذه التطعيمات ؟
وكيف يتحصل المريض علي مناعة ممتدة طول العمر
وشفاءٍ تام من المرض؟
أولاً: عند حدوث الكي:
1.يتحطم الأنتيجين{الجسم الغريب المسبب للمرض}ْ بالحرارة المتحصلة من الكي بالماء المغلي تحطما جزئياً
2.وتبقي شفرته الوراثية المميزةً له في شكل الخيوط الأنتيجينية التي تلتصق بها سلاسل الأمينو أسيد، والبروتين الشفري الحامل لهذه السلاسل،{قلت المدون كل ماكتب باللون الاصفر هو شرح للتكنيك المناعي لكيف تتكون مناعة ضد السرطانات الجلدية والامراض البكتيرية والفطرية والفيروسية المزمنة والريكتيسيات} ...
= حيث تحتوي مادة ال(دي إن أي-DNA) والتي توجد في نواة الخلية سواء البشرية أو الأنتيجينية علي أُس التركيب الجيني في الكروموزومات هذا الأس المعروف بأربعة حروف فقط هي (A , G ,T , C ) وبهذه الحروف الأربعة تكتب كل المعلومات المخزنة في هذا شيفرة الخلية وتتركب صفات كل مخلوق من الأحياء بعمليات توافيق وتباديل محسوبة بدقة ربانية بين هذه الأسَّات البروتينية الأربعة حسب ترتيب كل من A , G , T , C مجموعات من الفوسفات Phosphate Groups وقواعد الأدنينAdenin (A) , والثيامين Thymine (T),والجوانين Guanin (G), والسيتوسين Cytosine ©النيتروجينية.)،
وحيث تكون الجينات التي تحمل جميع الصفات الوراثية للكائن الحي ,وقد أمكن التعرف على الخارطة الوراثية:( الجينوم البشري) لكثير من الكائنات الحية , ودراستها ويعتبر هذا فتح علمي عظيم لحل العديد من المشكلات الوراثية للكائنات الحية|و"يبلغ عدد الجينات في جسم الإنسان في المتوسط حوالي 30 ألف جين (اختُلِف فى عدد الجينات البشرية فهناك من يقول انها ما بين 30 الى 140 الف جين وهناك من يقول انها 38 وهناك من يقول انها 100 الف ) كل جين يختص بتركيب جزء في الجنين و اى خطأ في حرف واحد شفري في هذا السجل يظهر على شكل عيب ولادي(خلقي تجاوزا في التسمية) أو مرض وراثي، ولو فرضنا أن هذه المعلومات تخص الإنسان فإنه بهذه الحروف الأربعة وبعملية توافيق وتباديل معجزة يُكتب لون البشرة, ولون العيون والشعر وصفاته وعدد شعراته, والحواجب, وفتحات الفم, والأسنان وتركيبها وترتيبها, والشفتين والأذنين وخصائص كل منها وكيف تعمل, وشكل الوجه, وعدد العظام به , والحلق وما به من خلايا وتراكيب, واللسان وطوله وشكله وخصائصه الوراثية والتشريحية والوظائفية, واللوزتين وعملهما والحلق, والغدد اللعابية, والبلعوم والمريء والمعدة, والرأس والمخ والخلايا العصبية, وكل المعلومات التي تعرفها عن جسم الإنسان والتي تدرس بالتفصيل في كليات الطب ومراكز البحوث , كل ذلك مكتوب في الشريط الوراثي الذي يتكون من خيطين دقيقين كيميائيين يتركبان من السكر الخماسي منقوص الأوكسجين (Deoxyribose sugar ) يرتبط بمجموعات من الفوسفات Phosphate Groupsوقواعد الأدنين Adenin (A) , والثيامينThymine (T), والجوانين Guanin (G),والسيتوسين Cytosine © النيتروجينية. يلتف حول نفسه ليكون شريط مزدوج بدلا من بقائه شريط منفرد ،فقد خلق بأن يكون التفافا متقنا ومحددا فكل عشرة نيوكليوتيدات تلتف لفة/وعلى حسب ترتيب كل من A , G , T , C تتكون الجينات التي تحمل جميع الصفات الوراثية للكائن الحي
مما يتكون هذا الشريط الشفري الجينومي الوراثي؟؟
لقد أثبت علماء الوراثة أنه يتكون من تتابع متسلسل من القواعد النيتروجينية تعارف العلماء علي أنها أربعة قواعد نيتروجينية يرمز لها بالحروف a.t.c g وعدد هذه القواعد في الجينوم البشري ما يقارب من 3 مليارات قاعدة نيتروجينية ومما أدهش العلماء أن هذه القواعد تتشابه في تتابعها بنسبة 9.99% في كل بني البشر ونسبة الاختلاف لا تزيد علي .1% وهذه النسبة الضئيلة هي التي تفرِّق بين مخلوق وآخر فهذا أسود وذلك أبيض وتلك جميلة والثانية عادية إلي ما لا نهاية من الاختلافات الموجودة بين البشر بحيث لا تجد واحداً يتشابه بها كاملاً مع آخر
ولم يجد العلماء علي مستوي الشخص الواحد اختلافاً في تركيب المادة الوراثية في هذا الشريط فكتاب الحياة الموجودة في خلية العين هي نفسها الموجودة بنفس التركيب في خلية القلب مثلاً أو العضلات أو الدم ولكن الإعجاز الإلهي يتجلي فيما شاهده العلماء حيث وجدوا جينات تكوين الدم موجودة علي كتاب حياة خلايا العين ولكنها متوقفة ولا تعمل في العين وتعمل في الدم فقط وهذا بقدرة الله الواحد المتعال ولقد أدرك العلماء ايضا أن الجينات في أي خلية في الجسم ليست كلها نشطه في جميع الأوقات ، فقد تنشط بعض الجينات في فترة ما ثم تدخل في مرحلة من عدم النشاط . كما يتم تعويق بعض الجينات في بعض اللحظات ويسمح للبعض الآخر بالعمل
و هناك أيضا جينات لا تعمل في بعض خلايا الجسم بينما تعمل في خلايا أخرى . فعندما ركز فريق من العلماء أعماله على الجينة الرئيسية التي تقود عملية تشكيل العين والرؤية ، وجدوا هذه الجينة لا تؤدى عملها بشكل طبيعي سوى في الخلايا المتواجدة في مكان العيون كما وجدوا أن الجينات المسؤوله عن تكوين إنزيم الببسين تكون نشطه في خلايا بطانة المعدة حيث أن إفراز إنزيم الببسين ضروري لهضم البروتينات في المعدة ، بينما هذه الجينات تجدها خامدة في باقي خلايا الجسم . كذلك فإن جينات إنتاج هرمون الأنسولين تكون نشطه في خلايا بيتا في جزر لانجرهانز في البنكرياس ، حيث أن هذه الخلايا هي التي تفرز هذا الهرمون الضروري للتعامل مع سكر الجلوكوز في الدم، بينما نجد أن هذه الجينات خامدة في باقي خلايا الجسم وهكذا
ولقد اكتشفوا أن كل خلايا الكائنات الحية،سواء منها الإنسان أو الذبابة أو دودة الأرض تمتلك في نواتها جميع الجينات التي تسمح بنمو كائن مشابه من الكائنات الأخرى بغض النظر عن نوعه ولكنها لا تقوم بذلك العمل لكونها في حالة سبات.
والغريب أن من ضمن هذه الجينات الجينات المسببة لمرض السرطان و التي تكون خامدة وكامنة وليس لها فعل أو دور في الظروف العادية بينما تنشط في ظل بعض العادات السيئة مثل إدمان التدخين أو إدمان الخمور أو بسبب أشياء أخرى مثل المبيدات و التعرض للإشعاع وإذا كان هناك جينات تسبب مرض السرطان فهناك أيضا جينات تحد من انتشاره وقد تم اكتشاف بعضها. والجين عند نشاطه يتم نسخه إلى حمضRNA، وعلى ذلك فإن حمض DNA في نواة الخلية لا يتم نسخه باستمرار ولكن فقط أجزاء منه هي التي تنسخ وذلك لبعض الوقت .[قلت المؤلف: وهذا سيفسر لنا تعامل الجهاز المناعي مع الكسرات الشفؤية التي أحدثناها بتعريض جزء من منطقة الإصابة التي تم كيِّها بالماء المغلي كما سبق وصفه قبل صفحات من هنا ] لقد قام فريق مشترك من الباحثين البلجيكيين والسويسريين برئاسة البروفيسور (وولتر غيرسرينغ) مدير المختبر البيولوجي الحكومي في جامعة بال بعد أربع سنوات من الأبحاث والتجارب ساهموا في اكتشاف ذبابة تحتوى على أربع عشرة عيناً متموضعة في أماكن مختلفة ، منها على الأجنحة وبعضها على القائمين وأخرى على قرون الاستشعار ، وأن خلايا الكائنات الحية جميعا ، سواء منها الإنسان أو الذبابة أو دودة الأرض تمتلك في نواتها جميع الجينات التي تسمح بنمو كائن مشابه ، ولكنها لا تقوم بهذا العمل لكونها في حالة سبات.إذن فالشريط الوراثي (DNA) لا يحمل المعلومات الخاصة فقط بالكائن الذي ينتمي إليه بل يحمل كل المعلومات المتعلقة بالكائنات الأخرى وصفاتها |وفي عملية تخليق البروتين التي تتم تحت إشراف ال(DNA) وبتوجيه إلهيٍ منه مع مشاركة ثلاثة أنواع أخرى من الأحماض النووية يطلق عليها الأحماض النووية الريبوزيه وهى :
1.الحمض النووي الريبوزي الرسول messenger RNA or m-RNA
2.الحمض النووي الريبوزي الناقل transfer RNA or t-RNA | 3.الحمض النووي الريبوزي الريبوسوميribosomal RNA or r-RNA
^^وتتعاون هذه الأحماض النوويه الريبوزيه معا فى تناسق معجز وبالطبع تحت إشراف ال(DNA) لتخليق سلاسل الأحماض ألأمينيه المكونة للبروتين ،
فكل حمض من هذه الأحماض النووية الريبوزيه له دور معين في عمليه تخليق سلسلة الأحماض ألأمينيه RNAالرسول (m-RNA) - ينسخ RNA من أحد شريطيDNA بواسطة أنزيم بوليميريز polymerase) من عند تتابع النيكلوتيدات علىDNA يسمى المحفز...
حيث ينفصل شريطي DNA عن بعضهما حيث يعمل أحدهما كقالب لبناء m-RNAويكون القالب في اتجاه 3-5 فيقوم الأنزيم ببناءm-RNA في اتجاه 5-3
وتضاعف DNA يتم في كلDNA بينما نسخ m-RNA يتم في جزء من DNAيمثل جين، تضاعف DNA يتم في كلٍ من شريطيDNA بينما m-RNA يتم نسخه من خلال شريطDNA واحد فقط.
^يدل توجيه المحفز على الشريط الذي سينسخ وهو الذي يبدأ بكودون (TAC) علىDNA ليتكون على m-RNA كودون (AUG- يوجد في أوليات النواة أنزيم بلمرة RNA ينسخ كل أنواعRNA الثلاثة أما في حقيقيات النواة فيوجد أنزيم لنسخ كل نوع منها..في عقل النواة يتم ترجمة m-RNA إلى البروتين المقابل في أثناء نسخة منDNA، بينما في أعماق النواة لا تبدأ الترجمة أي تخليق البروتين المقابل الا بعد الانتهاء من نسخ m-RNA وخروجه من النواة إلى السيتوبلازم.
في بداية كل m-RNA يوجد موقع الارتباط بالريبوسوم وهو تتابع للنيوكليوتيدات برتبط بالريبوسوم بحيث يصبح أول كودون AUG متجهًا لأعلى وفي نهاية m-RNAيوجد ذيل متعدد الادينين (يتكون من حوالي 200 أدينوزين) يعمل هذا الذيل لحماية m-RNA من التحلل في السيتوبلازم بواسطة الأنزيمات الموجودة فيه. 2- RNA الريبوسومي (r-RNA) - يدخل في تكوين الريبوسومات (أماكن بناء البروتين في الخلية) عدة أنواع من r-RNA (4 أنواع من r-RNA) , وحوالي 70 نوعًا من عديد الببتيد
يتم بناء الريبوسومات في النوية ويكون بالآلاف كل ساعة ويكون معدل الإنتاج سريعًا لاحتواء DNA في أرجاء النواة على ما يزيد من 600 نسخة من حينات إنتاجr-RNA.
- يتكون الريبوسوم من تحت وحدتين(subunit )أحدهما كبيرة والأخرى صغيرة.
- تكون تحت الوحدتين(subunit ) منفصلين في حالة عدم إنتاج البروتين وترتبط كل تحت وحدة(subunit ) كبيرة بتحت وحدة(subunit) صغيرة عند بدء تكوين البروتين.
- يتم بناء
البروتينات التي تدخل في تركيب الريبوسومات في السيتوبلازم ثم تنتقل إلى النواة
عبر الغشاء النووي المثقب حيث تتكون الريبوسومات.
- أثناء إنتاج البروتين يحدث تداخل بين m-RNA وr-RNA وطبيعة هذا التداخل
غير مفهومة حتى الآن. 2- RNA النقل
(t-RNA)
3- RNA الناقل (RNA-t)
- يقوم t-RNA
بنقل الأحماض الأمينية إلى الريبوسومات.| - لكل حمض
أميني t-RNA ناقل خاص به يقوم بنقله.|- الأحماض
الأمينية التي لها أكثر من شيفرة يكون لها أكثر من نوع من( t-RNA ) لذا يكون عدد( t-RNA ) أكثر من
عشرين |ينسخ t-RNA من جينات على DNA توجد في تجمعات من 7-8 جينات على نفس الجزء من DNA.
- يلتف t-RNA بحيث تكون
هناك أجزاء مفردة وأخرى مزدوجة.
^يوجد موقعان على t-RNA لهما دور في تخليق البروتين.
^الموقع الأول CCA يوجد عند الطرف وهو الخاص بالارتباط مع الحمض الأميني الخاص به.
^الموقع الآخر هو مقابل الكودون الذي تتزاوج قواعده مع قواعد m-RNA بحيث يحدث ارتباط مؤقت بين t-RNA و m-RNA مما يسمح للحمض الأميني المحمول على t-RNA بالدخول في سلسلة عديد البيتيد.
الكورموسومات الكورموسومات هي التي تحمل الجينات وتتركب من:
^الحمض النووي dna الذي يتكون من هيكل السكر فوسفات والقواعد النتروجينية على هيئة سلم حلزوني ملتف حول نفسه هيكله السكر فوسفات ودرجاته القواعد ويبلغ عدد القواعد التي يحتويها الشريط الوراثي أو الكورموسوم 6,2 مليار قاعدة تنتظم في 3,1 مليار زوج
^البروتينات، وهذه البروتينات تلعب دورًا مهمًا في المحافظة على هيكل المادة الوراثية، وتنظم نشاط تعبير الجينات الذي يؤدي إلى تكشف وتكوين الفرد الكامل من خلية الزيجوت.. وتكمن المعلومات الوراثية لأي خلية من تتابع الشفرة الوراثي (تتابع القواعد النيتروجينية الأربعة التي وهبها الله للحياة، وهي
1. الأدينين (A)
2. والجوانين (G)
3. والسيتوزين ©
4. والثيامين (T)
التي تكون المادة الوراثية في صورة كلمات وجمل تقوم بتخزين المعلومات الوراثية في لوح محفوظ مسئول عن حياة الفرد|يلاحظ أنه يدخل في تركيب كل كروموسوم جزيء واحد من DNA يمتد من أحد طرفيه الى الطرف الاخر الا انه يلتف وينطوي على نفسه عدة مرات ويرتبط بالعديد من البروتينات مكونا مايسمى بالكروماتين والذي يحتوي عادة على كمية متساوية من كل من البروتين وdna|تنقسم البروتينات التي تدخل في تركيب الكروموسومات إلى نوعين:
- هستونية histone
- غير هستونية nonhistonic
اولا : البروتينات الهستونية: هي مجموعة محددة من البروتينات التركيبية الصغيرة والتي تحتوي على قدر كبير من الحمضين القاعديين : ارجنين(Arginin) و ليسين| (Lysine)وتوجد الهستونات بكمية ضخمة في كروماتين اي خلية|ثانيا : البروتينات غير الهستونية: هي مجموعة غير متجانسة من البروتينات ذات وظائف عديدة مختلفة فهي تشمل بعض البروتينات التركيبية التي تلعب دورا رئيسيا في التنظيم الفراغي لجزيءDNA داخل النواة, كما تشمل بعض البروتينات التنظيمية التي تحدد ما اذا كانت شفرة dna ستستخدم في بناءRNAوالبروتينات والانزيمات ام لا|ويلاحظ أنه: يلتف جزئ DNA في الكروموسوم حول مجموعات من الهستون مكونا حلقات من النيوكليوسومات مما يؤدي الى تقصير طول جزيء DNA عشر مرات, الا انه يتعين ان يضم الجزيء ويقصر حوالي 100000 مرة حتى تستوعبه النواة ,, ولهذا فإن حلقات النيوكليوسومات تلتف مرة اخرى لتنضم مع بعضها البعض, ومع ذلك فإن كل ماسبق ليس بكاف لتقصير جزيء DNA الى الطول المطلوب(طول DNAمفرود يصل الى 2متر ونواة الخلية قطرها من 2الى 3ميكرون) تترتب اشرطة النيوكليوسومات الملتفة بشدة على شكل حلقة كبيرة بواسطة البروتينات غير التركيبية للكروماتين .) - وهكذا
فما علاقة الشرح السابق بتكوين مناعي مضاد للخلايا السرطانية الموجودة علي الجلد؟؟
فبعد هذه النبذة عن التكوين الشفري لل(دي-إن-إي)،يتبين أن الأجزاء المكسرة في مكان الكي كلها لها صفات وراثية بقواعدها البروتينية: الأدينين (A)والجوانين (G) والسيتوزين©،والثيامين (T)) ونواقله الكيمائية السابق تعريفها،
^وكل ما هو شفري حتي بعد تحطمه مكان الكي ، يقوم الجهاز المناعي للإنسان بخلاياه الكثيرة والمتنوعة بالتزاحم حول هذه الكسرات الأنتيجينية الوراثية والشفرية،كما لو أنه قد دعي إلي وليمة يتهافت كل نوع من الخلايا علي ما كلف به (سيأتي بمشيئة الله تعالي شرح تفصيلي لوظائف الخلايا المناعية وعمل كل واحدة منها هنا)،ثم يتشبع كل نوع من الخلايا المناعية بالتعرف بطريقته علي الكِسرات الشفرية((Genetic fragmentes، للأنتيجين ،ويطبعونه ويصورونه ويحفظون ذلك في ذاكرة خلاياهم، ثم تعود كل خلية إلي مهد إدارتها في نخاع العظام ومولِّدات الخلايا البيضاء في الجهاز الليمفاوي في الجسم. لتبدأ سيمفونية التصنيع الخلوي والهيوميرالي(المختلط)،الرائعة،المضاد للانتيجين كخلايا السرطان والفطريات والريكتسيات والبكتيريا المزمنة
فكيف يحدث ذلك؟؟
أولاً:التفاعلات الجلدية المناعية
أولا/ نبذة سريعة عن وظيفة الجلد المناعية
وظيفة الجلد المناعية: الجلد هو حاجز بيئي يبدأ بالاستجابة المناعية للأجسام الغريبة الثاقبة (الداخلة فيه) وهذا يؤدي إلى: تخرب العضويات الالتهابية.تعديل وإزالة السموم القوية والأنسجة المتأذية.
والجلد يحتوي أيضا على بعض العناصر من الجهاز المناعي الذي قد تشير إلى النسيج اللمفاوي المرافق للجلد(SALT ) وجهاز الجلد المناعي (SIS ).
وتحوي بشرة الإنسان خلايا لا نجرهانز والخلايا الكيراتينية التي عندما تثار سوف تشكل عدة أنواع من الستيوكينات التي تنقل وتحرض تكا ثر وتنمي اللمفاويات والبالعات الكبيرة (Macrophages) والتي تساهم وتحرض وتثير الحساسية. وظائف الجهاز المناعي في الجلد مثل الأعضاء الأخري في الجسم هي :
1.إما غير نوعية
2.أو نوعية.
الجهاز المناعي اللا نوعي ( Non specific immune system ) ، الآلية المناعية اللا نوعية هي الخط الأول من دفاع الجسم عندما يتعرض للمستضد. وتشمل:دفاع فيزيائي يقوم به الجلد. مفرزات الجسم ( المخاط ـ الأهداب في المجاري التنفسية. الغدد الد هنية ومفرزاتها).خلوية: هي تنجز بواسطة البالعات والخلايا القاتلة الطبيعية |(NK ) الجهاز المناعي النوعي (Specific immune system):،هذا النمط له دوره عندما يفشل الجهازالمناعي اللانوعي من التخلص من المستضد(Antigen) المهاجم. هذا الجهاز يشمل المركبات الخلوية (Cellular) والخليطة(Humoral) التي تملك ذاكرة مناعية نموذجية حيث أنه يحرض استجابة مناعية بتكرار التعرض لنفس المستضد. وظائف الجهاز المناعي النوعي: الجهاز المناعي النوعيى ينتج الخلايا المناعية وهي:
أ)خلايا البائية "B"
ب)والخلايا التا ئية "T"
الخلايا التائية:تساهم في كل من الاستجابة المناعية الخلويه والخليطة.
الخلايا البائية: تنتج مجموعات أضداد"غلوبولينات" مناعية مختلفة:" IgE , IgG و IgM, Ig A و"IgD".
^التفاعل الألرجي قد يعزى إلى عوامل داخلية المنشأ أوخارجية المنشأ.
ا ـ المستضد"Antigen ": هو مادة غريبة يمكنها أن تثير استجابة مناعية. وهذا قد يؤدي إلى:تشكيل الأضداد "Antibodies".
تغير فعالية الخلايا اللمفاوية المعروفة باسم الاستجابة المتواسطة بالخلايا "Cell mediated response
الصفات الكيماوية للمستضدات: قد تكون المستضدات صغيرة الوزن الجزيئي أو كبيرة الوزن الجزيئي
1-المستضدات كبيرة الوزن الجزيئي (High molecular weight antigens): تتشكل من الأحماض الأمينية والببتيدات التي يمكنها أن تثير وتحرض تكوين الأضداد
2- المستضدات صغيرة الوزن الذري(Low molecular weight antigens) : هذه الأنواع لاتستطيع أن تحرض تشكيل الأضداد مالم ترتبط مع بروتين، هذه تعرف باسم (النواشب) Haptens ويمكن أن تثير الأضداد الخليطة Humoral أو النمط المتأخر (المتواسط بالخلايا :Delayed cell type ) من الحساسية التي تكون نوعية للنواشب.
المستضدات التي تحسس الأشخاص بشكل أكثر شيوعاً للحساسية الاستهدافية(Anaphylactic) أو النمط المتأخر وهذا يعرف باسم مستْارج "الرياجين" أو مولد الارجيه(Allergen) .
الأضداد|(Antibodies) :هي جلوبولنيات مناعية مصلية تتشكل استجابة لتحريض المستضد.
^والأضداد تتشكل من قبل الخلايا البلازمية
^وتتألف من سلاسل عديدة من بولي ببتايدات.
^الوحدة الرئيسية للضد هي جزيئ الجلوبولين المناعي (Ig):يوجد عدة جلوبولينات مناعية في المفرزات الخارجية مثل القناة المعوية والطرق التنفسية.
^فشل أي جزء من جهاز المناعة قد يؤهب للتحسس، أو إلى الالتهاب أو إلى الأمراض الخبيثة.
التفاعلات المناعية المختلفة: تفاعل ضد ـ مستضد : (Antigen-antibody reaction) ، سواء كان تفاعلاً فورياً يحدث بعد التعرض لمستضد معين أو من نمط التفاعل المتأخر.
التفاعلات الأرجية الفوريه: (نمط I, II, III) وهي تمثل استجابة خلطية "Humoral"وتشابه خلايا تائية" او B-lymphocytes "مثارة وكذلكالخلايا المصورية(Plasma cells) التي تنتج وتنشط الجلوبولينات المناعية المختلفة.
التفاعل الأرجي المتأخر ( ،نمط IV ) قد يستغرق التفاعل الأرجي عدة ساعات أو أيام أو حتى أسابيع ليظهر من وقت التعرض للمستضد. هذا النمط متواسط بالخلايا(Cell medited) بواسطة اللمفاويات من نوع (T-lymphoctes) التائية المتحسسة.
تفاعلات فرط الحساسية المختلفة: حسب تصنيف "جيل وكومبس ( Gell & Coombs) هي:
1.النمط الفوري ـ الاستهدافي اؤ التأقي: "Immediate or anaphylactic reaction |قد يكون المستضد من الأطعمة، حبات الطلع، الغبار، الريش، أو غيرها.الأضداد: هي الجلوبولينات المناعية IgE .
2.تفاعل ضد ـ مستضد: (Antigen-antibody reaction)يسبب زوال تحبب الخلايا الدقلية أو البدنية(Degranulation of Mast cells) حيث يؤدي ذلك إلى تحرر عدة وسائط خاصة مثل:الهيستامين، سيروتونين، البراديكنين والمواد البطيئة(SRS)
^المظاهر الفيزيائية التشريحية المرضية التي تحدث نتيجة لذلك هي :
أ)توسع الأوعية الدموية.
ب)زيادة النفاذية الوعائية.
ج)تقلص العضلات الملساء.
المظاهر السريرية للنمط، هي:
1. شري
2. وذمة وعائية
3. صدمة ثاقبة
4. ربو قصبي
5. والتهاب أنف أرجي.
2.نمط الأضداد السامة للخلايا (النمط)
Cytotoxic antibody II
( المستضد: في التفاعل الأرجي نمط الثاني هو (Hapte) الناشب الذي: 1.يترسب على جدر الخلية
2.أو على الأغشية الخلوية التي تعمل كمستضد
الأضداد:
هي أضداد سامة للخلايا من الأصناف" IgA , IgG وIgM يحدث التفاعل الأرجي كنتيجة لتفاعل الأضداد الجارية مع الدورة الدموية أو الأضداد الخلوية مع المستضدات (الجارية) التي تؤدي إلى ارتباط المتممة مع معقد الضد ـ مستضد(Complement) مؤدياً إلى انحلال الخلايا المستهدفة.
تأثير كل تفاعل كهذا هو من النوع اغلال خلوي (Cytolysis).
المظاهر السريرية-الإكلينيكية- للتفاعلات السامة للخلايا هي :
1.نقص الصفيحات
2.فقر دم اغلالي(Hemolytic anemia
3.فرط المحبباتAgranuloctosis).
4.وأمراض المناعة الذاتية (Auto-immune diseases)
5.معقد ضد ـ مستضدcomplex)
،النمط/ III تفاعل آرثس (Arthus reaction).
المستضد: في هذا النمط يكون دواء ـ مصل غريب ومستضدات أخرى مثل العقديات والأروام.
^^الأضداد: في النمط (III ) من التفاعلات الأرجية هو "الجلوبولين المناعي: "IgG" والمتممة"
^^التفاعل الأرجي (Complement)يحدث كنتيجة لآلية معقدة.
^^التبدلات الفيزيوكيماوية التي قد تحدث نتيجة لهذا النوع من التفاعل: ترسب معقدات الضد- المستضد(Antigen-antibody reaction) على جدران الأوعية الدموية الشعرية.
^^ تفعيل نظام المتممة. انجذاب الكريات البيض وفرط البالعات(Phagocytosing cells) للمركب المناعي بواسطة الكريات البيض.
^^انحلال البالعات.
^^تخريب جدر الخلايا بالأنزيمات الليزوزومية.
()إن تأثيرات هذه التفاعلات هي التهاب ونخر(Necrosis) الانسجه.
المظاهر السريرية للتفاعلات الأرجية في النمط III هي(تفاعلات آرثس)(،ظاهرة آرتوس - داء المصل).
طفح الأدوية.
انحلال البشرة النخري السمي.( الحمامي المتعددة الأشكال) )Erythema multiforme)والحمامي العقدية( Erythema nodosum(
التفاعل المتأخر المستضد :(النمط IV) هو يشمل أنواعاًمختلفة من المواد الكيماوية وغيرها. الأضداد: هي اللمفاويات التائية
التفاعل الألرجي ينجم عن تفاعل مستضد ـ لمفاويات ناجم عن عوامل خليطة تؤدي إلى ظهورLymphokines (ليمفوكنيات.
تأثيرات هذه التفاعلات هي: توسع وعائي ـ وذمة ـ ارتشاح بالوحيدات واللمفاويات. المظاهر السريرية هي: أكزيما التماس الأ لرجية ـ أكزيما الضياء الألرجية ـ الطفوح الألرجية ورفض الأعضاء. المظاهر قد تكون موضعية في الجلد أو تصيب الجلد والأعضاء الأخرى.
-النمط العاجل والآجل للتفاعلات التحسسية هي مهمة جداً في آلية الأكزيما. التفاعل العاجل: يحدث بسبب زوال تحبب الخلايا البدنية(Mast cells) : بسبب التحريض من الضد المؤدي لتحرر الوسائط مثل: "الهيستامين، اليوكوترين، والعامل المفعل للصفيحات، البروتياز " وغيرها. وهذا التفاعل قد يؤدي إلى أمراض جلدية مثل المراحل الباكره من الأكزيما الاستشرائية(Atopic dermatitis) ، الشري والوذمة العرقية. اسقصاء هذا النمط هي: اختبارات الوخز ـ تعيين عيار "IgE "وتجربة المصل (RAST ). التفاعل الآجل: التماس المتكرر لمستضد معين مع الخلايا التائية المتحسسة سابقاً يؤدي إلى تحريض وتحرير " اللمفوكينات" التي تثير اتفاعلا التهابيا وتفعل البالعات الكبيرة لتحرر الوسائط. هذا النمط من التفاعل مسؤول عن النوع المتأخر من أكزيماالملامسة، الأكزيما الضوئية الأرجية والمراحل المتأخرة من الأكزيما الاستشرائية| (Atopic dermatitis). التفاعلات المناعية المتواسطة بالخلايا لها دور هام في المقاومه ضد الفطور، والفيروسات والانتانات الحبيبية للجلد والتفاعلاتالوسيطة للدغ الحشرات. اختبارات البقعة وتفاعل تشكيل اللمفاويات قد تفيد في تحديد العامل المسبب للحساسية.
وهكذا وبعد هذه النبذة عن كيفية عمل جهاز المناعة في الأحياء البشرية،.... يتبين لنا أن الأجزاء المكسرة في مكان الكي كلها لها صفات وراثية بقواعدها البروتينية:
1. الأدينين (A)
2. والجوانين (G)
3. والسيتوزين ©
4. والثيامين (T)
ونواقله الكيمائية السابق تعريفها، وكل ما هو شفري حتي بعد تحطمه مكان الكي ،
ثانيا /حيث يقوم الجهاز المناعي للإنسان بخلاياه الكثيرة والمتنوعة بالتزاحم حول هذه الكسرات الأنتيجينية الوراثية والشفرية، كما لو أنه قد دعي إلي وليمة يتهافت كل نوع من الخلايا علي ما كلف به،
ولعل ذلك يرجع إلي انتشار رائحة الكسرات الجينية للأتيجين المكسر في منطقة الكي علي الجلد المكوي،والتي تتشممها الخلايا المناعية الدوارة في الدم والموجودة في الأنسجة بجهاز شم معين(عن طريق النواقل الكيمائية التي يتملي بها جهاز المناعة ويذخر بها)،مما يؤدي إلي تهافت الخلايا المختلطة والخلوية(cellular and humeral)،
وتتداعي علي الكسرات الأنتيجينية لخلايا السرطان المدمرة علي الجلد،أو أي نوع آخر من الخلايا المرضية الموجودة علي الجلد،
أو ربما أدي التكسير الأنتيجيني للخلايا السرطان أو أي خلايا لمرض جلدي موجود في مكان الكي لسهولة تعرف الخلايا المناعية علي الشيفرة الجينية للأنتيجين بعد موته وتكسيره إلي أجزاء شفرية بعد كيِّه بمنطقة الحرق بالكي المائي، حيث كان قبل تكسر الأنتيجين ممتنعاً علي خلايا جهاز المناعة التعرف عليها (سيأتي بمشيئة الله تعالي شرح تفصيلي لوظائف الخلايا المناعية وعمل كل واحدة منها هنا)،
ثم يتشبع كل نوع من الخلايا المناعية بالتعرف بطريقته علي الكِسرات الشفرية((Genetic fragmentes، للأنتيجين ، ويطبعونه ويصورونه ويحفظون ذلك في ذاكرة خلاياهم،
ثم تعود كل خلية إلي مهد إدارتها في نخاع العظام ومولِّدات الخلايا البيضاء في الجهاز الليمفاوي في الجسم. لتبدأ سيمفونية التصنيع الخلوي والهيوميرالي(المختلط)،الرائعة.
ثالثا/ وفي الجزء الثاني بمشيئة الله تعالي نلقي في المدونة[أو الكتاب] بحزمة كبيرة ممتلئة بأسرار التفاعل المناعي علي سطح الجلد وكيف يؤدي ذلك إلي تمام الشفاء من السرطان بكل الجسم وليس فقط علي سطح الجلد وذلك في غضون عدة أشهر من بداية عملية الكي المائي الرطب،
كما سنناقش الطرق المختلفة للوصول بهذا التكنيك الرائع للسرطانات التي ليس لها ظهور علي سطح الجلد،
رابعا/ وما العلاج بالليزر الحارق للخلايا السرطانية إلا نموذجا حضريا لهذا التكنيك
وسيأتي طريقة تفعيل العلاج بالليزر في مثل هذا المجال بمشيئة الله تعالي، ووجوب تعاون أخصائيوا الجراحة العامة مع أخصائيي الجلد والمناعة في التواصي بعلاج السرطان خاصة بنفس التكنيك بحيث يقرب استشاري الجراحة العامة الطريق للمعالجين بالكي وذلك باستخراج جزء من النسيج السرطاني الكامن بالجسم بعد استئصاله الجراحي ويقوم بزرع جرافت منه تحت الجلد بعد تعريضه للماء المغلي ويلصق النسيج المعالج بالماء المغلي [والذي تم تكسير الخلايا الذاتية السرطانية به بالماء المغلي ] ثم يلصق بفتح بسيط جدا في الجلد في الطبقة تحت الجلدية وتخيط الغرز ويترك للتفاعل المناعي ويتم ذلك في حجرة العمليات أثناء استئصال الورم.
لَمْ يَكُنِ الَّذِينَ كَفَرُوا مِنْ أَهْلِ الْكِتَابِ وَالْمُشْرِكِينَ مُنْفَكِّينَ حَتَّى تَأْتِيَهُمُ الْبَيِّنَةُ (1) رَسُولٌ مِنَ اللَّهِ يَتْلُو صُحُفًا مُطَهَّرَةً (2) فِيهَا كُتُبٌ قَيِّمَةٌ ..
الدين القيم قال تعالي في دينه القيم : لَمْ يَكُنِ الَّذِينَ كَفَرُوا مِنْ أَهْلِ الْكِتَابِ وَالْمُشْرِكِينَ مُنْفَكِّينَ حَتَّى تَأْت...
-
وفاة النبي صلى الله عليه وسلم لأحمد بن شعيب النسائي (829–915) قاضي وأحد أئمة الحديث النبوي الشريف صاحب السنن الصغرى والكبرى ==========...
-
<p style="text-align: center;"><a href="https://fadlll.blogspot.com/2023/11/blog-post_85.html"><span...
-
العلماء ومسؤلياتهم الخطيرة علي ضياع دين الله في نفوس المسلمين وقلوبهم وعقولهم بإستقراء الأمور علي عقائدهم في واقعهم وقيام أعتي المو...
